Schleim-Moleküle können Pilzinfektionen vereiteln
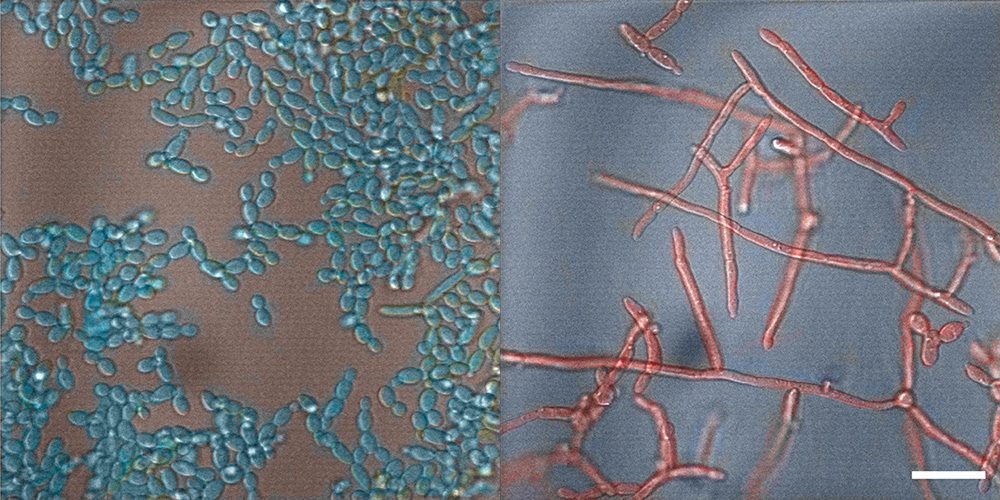
Candida albicans ist ein Pilz, der die Schleimhäute der meisten gesunden Menschen besiedelt. Unter bestimmten Bedingungen kann er in eine schädliche Form übergehen und Infektionen verursachen. Forschende haben nun Moleküle im Sekret der Schleimhäute identifiziert, die den Erreger daran hindern, schädlich zu werden, und legen damit den Grundstein für eine neue Klasse von Medikamenten.
Die meisten Menschen bemerken gar nicht, dass sie einen potenziell schädlichen Erreger in sich tragen. Dass sich Candida albicans nicht bemerkbar macht, verdanken sie zum Teil einer Substanz, die normalerweise nicht hoch im Kurs steht: Schleim. Das Sekret, das alle Schleimhäute des Körpers bedeckt, hält diesen Hefepilz in Schach. Doch welche Bestandteile des Schleims genau für seine erregerhemmenden Eigenschaften verantwortlich sind, war bisher unklar.
Ein internationales Forschungsteam mit Beteiligung von Dr. Rachel Hevey von der Universität Basel und Prof. Dr. Katharina Ribbeck vom Massachusetts Institute of Technology (MIT) hat diese Bestandteile identifiziert: spezialisierte Zuckermoleküle, Glykane genannt. Wie die Forschenden im Fachjournal Nature Chemical Biology berichten, können bestimmte Glykane die sogenannte Filamentierung von Candida albicans unterdrücken, also den Wechsel zur infektiösen Form.
Der Zucker im Schleim
Glykane sind ein Hauptbestandteil von Mucinen, den gel-bildenden Polymeren, aus denen Schleim besteht. Mucine enthalten viele verschiedene Glycane. Neuere Studien deuten darauf hin, dass diese spezialisierten Zuckermoleküle bestimmte Krankheitserreger im Zaum halten können.
Um zu testen, welche der mehreren hundert verschiedenen Glykane im Schleim mit Candida albicans interagieren, verglich die Forschenden die molekulare Zusammensetzung verschiedener Schleimproben, die in Laborversuchen die Filamentbildung des Pilzes unterdrückten. Von den Glykanen, die in allen Proben am häufigsten vorkamen, synthetisierten Rachel Hevey und ihr Team am Fachbereich Pharmazeutische Wissenschaften sechs für die weitere Analyse.
«Es ist fast unmöglich, Glykane aus Schleimproben zu isolieren», sagt Hevey. «Die einzige Möglichkeit, ihre Eigenschaften zu untersuchen, besteht darin, sie zu synthetisieren. Aber das ist ein äusserst komplexes chemisches Verfahren.» Sie und ihre Kollegen gehören zu den wenigen Forschungsgruppen weltweit, die eine Methode zur Synthese dieser Moleküle entwickelt haben.
Ribbeck und ihr Team am MIT konnten anschliessend die Wirkung der synthetisierten Glykane auf Candida albicans bestätigen. In Verbindung mit Ribbecks früheren und laufenden Arbeiten an anderen Krankheitserregern sind die Forschenden überzeugt, dass Glykane der Schlüssel zu einer neuen Klasse von Medikamenten gegen Pilzinfektionen (Antimykotika) sein könnten. «Es zeichnet sich ab, dass Schleim eine umfangreiche Bibliothek kleiner Moleküle mit vielen Virulenzhemmstoffen gegen alle möglichen problematischen Erreger enthält, die nur darauf warten, entdeckt und genutzt zu werden», sagt Ribbeck.
Nicht nur für «Schleimigkeit»
In seiner schädlichen Form kann Candida Erkrankungen wie Mundsoor, vaginale Hefepilzinfektionen oder sogar eine lebensbedrohliche systemische Infektion verursachen, die das Blut, das Herz und andere Teile des Körpers angreift und in etwa 40 Prozent der Fälle tödlich verläuft. Es gibt nur wenige Antimykotika, die Behandlung dieser Infektionen bleibt also eine Herausforderung.
«Es besteht ein dringender Bedarf an neuen Antimykotika», sagt Hevey. «Lange Zeit dachte man, dass Glykane nur für die ‹Schleimigkeit› des Schleims verantwortlich sind. Jetzt sehen wir, dass sie tatsächlich den Weg für neue, dringend benötigte Medikamente gegen problematische Krankheitserreger ebnen könnten.» Das Team sucht derzeit nach Möglichkeiten, Glykane zu verschiedenen Bereichen im Körper zu bringen.
Die Erkenntnisse beruhen auf der Zusammenarbeit eines Netzwerks von Forschenden mit einzigartigem Fachwissen, darunter Prof. Dr. Micheal Tiemeyer (Complex Carbohydrate Research Center, University of Georgia), Prof. Dr. Clarissa Nobile (University of California in Merced), Prof. Dr. Richard Cummings (Harvard Medical School) und Prof. Dr. Daniel Wozniak (Ohio State University).
Die Forschung wurde vom Schweizerischen Nationalfonds, den National Institutes of Health, der National Science Foundation und dem U.S. Army Research Office über das Institute for Collaborative Biotechnologies finanziert.
Quelle: Universität Basel